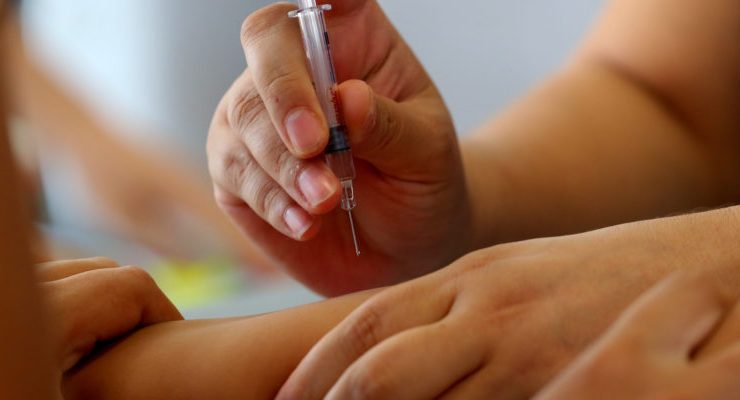
Los funcionarios federales de la salud votaron para aprobar las vacunas Oxford/AstraZeneca y Coronavac, dando inicio al proceso de vacunación en São Paulo este domingo. El país carioca es uno de los más golpeados por la pandemia.
(CNN en Español)– En medio de un devastador resurgimiento del coronavirus en partes de Brasil, funcionarios federales de salud del país sudamericano finalmente votaron para autorizar dos vacunas para uso de emergencia. El domingo, la agencia reguladora brasileña Anvisa aprobó tanto la vacuna Oxford/AstraZeneca como la vacuna Coronavac.
Minutos después, Monica Calazans, una enfermera negra del centro de São Paulo, se convirtió en la primera brasileña en vacunarse. Calazans, quien tiene un alto riesgo de complicaciones por covid-19 y trabaja en una unidad de cuidados intensivos (UCI) que ha estado al 90% de su capacidad o más desde abril, rompió a llorar antes de recibir la inyección de Coronavac.
“No saben lo que esto significa para mí”, le dijo al gobernador del estado de São Paulo, João Doria.
Brasil, el país más afectado de la región
Brasil es el país más afectado por el covid-19 en Latinoamérica. Ha registrado más de 8 millones de casos y más de 200.000 muertes por coronavirus. Si bien varios de sus vecinos ya han aprobado el uso de vacunas, Brasil parece estar rezagado a pesar de su reconocido historial de salud pública y vacunación.
La vacuna Coronavac, desarrollada por la empresa china Sinovac, ahora ha sido autorizada para el uso de 6 millones de dosis importadas. Tiene historia en el estado de Sao Paulo, donde el Instituto Butantan realizó ensayos clínicos de fase 3 de la vacuna. Butantan también producirá dosis futuras.
Lee también: Trump anunciaría cerca de 100 indultos como última acción de su presidencia
Sin embargo, Coronavac ha mostrado una tasa de eficacia media baja del 50,4%, apenas por encima del mínimo del 50% establecido por la Organización Mundial de la Salud. El número, que cae muy por debajo del 78% anunciado previamente, ha planteado dudas sobre la veracidad de los datos y ha alimentado el escepticismo sobre la aparente falta de transparencia con respecto a las vacunas chinas.
El informe técnico de Anvisa que dio luz verde a Coronavac subraya que la agencia también había tomado en cuenta la urgencia por el aumento vertiginoso de los casos de covid-19 en Brasil y “la ausencia de alternativas terapéuticas”.
También recomienda que se siga monitoreando la vacuna. Indica que el Instituto Butantan no había proporcionado datos importantes de su estudio de Fase 3, como la duración de la protección proporcionada por la vacuna y su efecto en los adultos mayores, personas con comorbilidades y otros grupos de pacientes.
Doria se ha comprometido a poner las vacunas desarrolladas en el estado a disposición del Ministerio de Salud federal de Brasil para su distribución nacional.
‘El Día V’
“Hoy es el Día V. Es el día de la vacuna, es el día de la verdad, es el día de la victoria, es el día de la vida”, dijo en rueda de prensa luego de que se aprobaron las vacunas. Fue un agudo golpe a la renuencia del ministro de Salud, Eduardo Pazuello, a comprometerse con una fecha de inicio de la vacunación a nivel nacional, que antes dijo que comenzaría “en el Día D y en la hora H”.
La vacuna Oxford/AstraZeneca, que mostró una eficacia promedio del 70,4% en los ensayos preliminares de Fase 3, también ha sido aprobada para el uso de 2 millones de dosis, que serán importadas del Instituto del Suero de la India por la Fundación Oswaldo Cruz de Brasil (Fiocruz).
Lee también: Vacunados con segunda dosis podrán saltarse el confinamiento en Israel
Fiocruz firmó un acuerdo para comprar y producir la vacuna con el gigante farmacéutico AstraZeneca en junio. Tras sucesivos retrasos, el gobierno brasileño firmó en octubre un contrato por 256 millones de dosis y anunció que recibiría las primeras en diciembre.
Después de otra serie de retrasos, Fiocruz espera recibir el primer envío a fines de enero.